Sulfonová kyselina

Jako sulfonové kyseliny se obvykle označuje třída organických kyselin, která má obecný vzorec R-SO2-OH, kde R je obvykle uhlovodíkový substituent. Termín sulfonová kyselina (resp. kyselina sulfonová) může označovat také konkrétního člena této třídy, kde R=vodík. Sulfonové kyseliny jsou příbuzné ke kyselině sírové, chybí jim jedna hydroxylová skupina.
Kyselina sulfonová

Kyselina sulfonová je méně stabilní tautomer kyseliny siřičité, na kterou se rychle přeměňuje. Odvozené sloučeniny, kde je vodík ve vazbě na síru nahrazen organickou skupinou, jsou stabilní.
Sulfonové kyseliny

Sulfonové kyseliny jsou obvykle mnohem silnější kyseliny než jejich karboxylové ekvivalenty a mají zvláštní schopnost těsně vázat bílkoviny a sacharidy; sulfonové kyseliny (nebo sloučeniny se sulfonylovou funkční skupinou) se proto používají jako „omyvatelná barviva“. Využívají se i jako katalyzátory a meziprodukty pro mnoho různých chemických produktů.
Sulfonové kyseliny a jejich soli (sulfonáty) se široce používají v různých výrobcích, například čisticích prostředcích, antibakteriálních sulfonamidech, anexových pryskyřicích (k čištění vody) a v barvivech.
Nejjednodušším příkladem je kyselina methansulfonová (CH3SO2OH), používaná jako reagencium v organické chemii. Důležitým reagenciem je také kyselina p-toluensulfonová.
Sulfonové estery
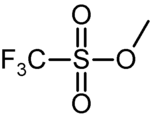
Sulfonové estery (estery sulfonových kyselin) je třída organických sloučenin s obecným vzorcem R-SO2-OR. Tyto estery, například methyltriflát (methyltrifluormethansulfonát, methylester kyseliny trifluormethansulfonové) se považují za dobré odstupující skupiny v nukleofilní alifatické substituci.
Sulfonylhalogenidy
Sulfonylhalogenidové skupiny se objevují v případech, kdy se sulfonylová funkční skupina váže (jednoduchou vazbou) na atom halogenu. Mají obecný vzorec R-SO2-X, kde X je halogen.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Sulfonic acid na anglické Wikipedii.
Literatura
- J.A. Titus, R. Haugland, S.O. Sharrow and D.M. Segal , Texas red, a hydrophilic, red-emitting fluorophore for use with fluorescein in dual parameter flow microfluorometric and fluorescence microscopic studies. J. Immunol. Methods 50 (1982), pp. 193–204.
- C. Lefevre, H.C. Kang, R.P. Haugland, N. Malekzadeh, S. Arttamangkul, and R. P. Haugland, Texas Red-X and Rhodamine Red-X, New Derivatives of Sulforhodamine 101 and Lissamine Rhodamine B with Improved Labeling and Fluorescence Properties, Bioconj Chem 1996, 7(4):482-9
Související články
- Kyselina sírová H2SO4
- Kyselina siřičitá H2SO3
- Karboxylové kyseliny
Externí odkazy
 Obrázky, zvuky či videa k tématu sulfonová kyselina na Wikimedia Commons
Obrázky, zvuky či videa k tématu sulfonová kyselina na Wikimedia Commons
| Funkční skupiny | |
|---|---|
| Aldehyd • Alkan • Alken • Alkohol • Alkoxy • Alkyn • Amid • Amin • Azosloučenina • Benzen a deriváty • Diazoniová sůl • Disulfid • Ester • Ether • Halogenderiváty • Imid • Imin • Isokyanid • Isokyanát • Karboxylová kyselina • Karboxymethyl • Keton • Kyanát • Nitril • Nitrosloučeniny • Nitrososloučeniny • Peroxid • Pyridin a deriváty • Sulfony • Sulfonová kyselina • Sulfoxid • Thioaldehyd • Thioester • Thioether • Thiol | |
| uhlovodíkové skupiny | Methylen • Methyl • Ethyl • Propyl • Propan-2-yl • Butyl • Pentyl • Ethenyl (vinyl) • Allyl • Fenyl • Benzyl • Tolyl • Naftyl • Alkyl (alkanyl) • Alkenyl • Alkynyl |
| acylové skupiny | |











