Hypochlorite de sodium
| Hypochlorite de sodium | |||
 | |||
 | |||
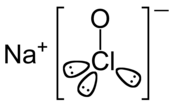
| Structure de l'hypochlorite de sodium | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | hypochlorite de sodium | ||
| No CAS | 7681-52-9 | ||
| No ECHA | 100.028.790 | ||
| No CE | 231-668-3 | ||
| PubChem | 23665760 | ||
| SMILES | [O-]Cl.[Na+] PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/ClO.Na/c1-2;/q-1;+1 Std. InChIKey : SUKJFIGYRHOWBL-UHFFFAOYSA-N | ||
| Apparence | solide blanc | ||
| Propriétés chimiques | |||
| Formule | ClNaONaClO | ||
| Masse molaire[1] | 74,442 ± 0,002 g/mol Cl 47,62 %, Na 30,88 %, O 21,49 %, | ||
| Propriétés physiques | |||
| T° fusion | 18 °C | ||
| Solubilité | 293 g·L-1 à 0 °C; 799 g·L-1 à 25 °C dans l'eau | ||
| Précautions | |||
| SGH[2],[3] | |||
  Danger H314 : Provoque de graves brûlures de la peau et des lésions oculaires H400 : Très toxique pour les organismes aquatiques EUH031 : Au contact d'un acide, dégage un gaz toxique P260 : Ne pas respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols. P301 : En cas d'ingestion : P303 : En cas de contact avec la peau (ou les cheveux) : P305 : En cas de contact avec les yeux : P330 : Rincer la bouche. P331 : NE PAS faire vomir. P338 : Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P351 : Rincer avec précaution à l’eau pendant plusieurs minutes. P353 : Rincer la peau à l’eau/se doucher. P361 : Enlever immédiatement les vêtements contaminés. P405 : Garder sous clef. P501 : Éliminer le contenu/récipient dans … | |||
| SIMDUT[4] | |||
   C, E, F, C : Matière comburante cause ou favorise la combustion d'une autre matière en dégageant de l'oxygène E : Matière corrosive forme au contact de l'eau une substance corrosive F : Matière dangereusement réactive devient autoréactif sous l'effet d'une augmentation de la température Divulgation à 1,0% selon la liste de divulgation des ingrédients | |||
| Transport[3] | |||
Code Kemler : 80 : matière corrosive ou présentant un degré mineur de corrosivité Numéro ONU : 1791 : HYPOCHLORITE EN SOLUTION contenant plus de 7 pour cent de chlore libre Classe : 8 Étiquette :  8 : Matières corrosives Emballage : Groupe d'emballage II/III : matières moyennement/faiblement dangereuses. | |||
| Inhalation | Dangereuse, peut être mortelle | ||
| Peau | Irritant, provoque des brûlures, peut être mortel | ||
| Yeux | Irritant, provoque des brûlures | ||
| Ingestion | Dangereuse, voire mortelle | ||
| intraveineuse | Irritant, provoque des infections | ||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
L’hypochlorite de sodium est un composé chimique de formule brute NaClO. C'est un solide blanc très instable couramment utilisé en solution aqueuse comme agent désinfectant et agent de blanchiment, notamment sous forme d'eau de Javel pour un usage domestique. Sous forme solide anhydre, il tend à se dismuter en oxygène O2, chlorure de sodium NaCl et chlorate de sodium NaClO3 :
Dans l'eau de Javel, l'hypochlorite de sodium est mélangé avec du chlorure de sodium résultant de sa fabrication par l'action du dichlore Cl2 sur une solution d'hydroxyde de sodium NaOH électrolysée entre deux électrodes rapprochée en dessous de 40 °C, afin d'éviter la formation de chlorate de sodium NaClO3 :
Réactions

L'hypochlorite de sodium réagit progressivement avec les métaux en donnant l'hydroxyde ou l'oxyde de ce métal, par exemple ici avec le zinc :
Il libère du dichlore gazeux Cl2 avec l'acide chlorhydrique HCl :
Avec les autres acides, il libère l'acide hypochloreux HClO, par exemple ici avec l'acide acétique CH3COOH :
- NaClO + CH3COOH → HClO + CH3COONa.
Sous l'effet de la chaleur ou de la dessiccation, il se dismute en chlorure de sodium NaCl et chlorate de sodium NaClO3 ou en oxygène O2 :
La réaction — violente — avec le peroxyde d'hydrogène H2O2 libère de l'oxygène singulet 1O2, défini par une configuration électronique particulière, notée 1Δg :
- NaClO + H2O2 → NaCl + H2O + 1O2↑.
Avec l'ammoniaque NH4OH, la réaction conduit à la formation d'hydroxyde de sodium NaOH et de monochloramine NH2Cl, toxique :
- NaClO + NH4OH → NaOH + NH2Cl + H2O.
L'hypochlorite de sodium rend l'eau de Javel dangereuse lorsqu'elle est en contact avec d'autres produits d'entretien ou divers produits d'utilisation domestique (par exemple des tensioactifs, des parfums d'intérieur...), car c'est un réactif instable qui forme facilement des composés nocifs, notamment des composés organiques volatils chlorés, avec de nombreuses substances de la vie quotidienne.
En chimie organique, on l'utilise pour oxyder les groupements -OH secondaires en présence de groupements -OH primaires. L'oxydation vers la cétone se fait en solution aqueuse avec de l'acide acétique[5].
Références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ Numéro index 017-011-00-1 dans le tableau 3.1 de l'annexe VI du règlement CE N° 1272/2008 (16 décembre 2008)
- ↑ a b et c Entrée « Sodium hypochlorite; solution ... percent Cl active » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 13 avril 2011 (JavaScript nécessaire)
- ↑ « Hypochlorite de sodium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- ↑ (en) George S Zweifel et Michael H Nantz, Modern organic synthesis : an introduction, New York, W.H. Freeman, , 477 p. (ISBN 978-0-7167-7266-8 et 0-7167-7266-3), p. 96.
v · m | |
|---|---|
| Dérivés de l'acridine |
|
| Biguanides et amidines |
|
| Phénol et dérivés |
|
| Nitrofuranes |
|
| Composés organo-iodés |
|
| Dérivés de la quinoléine |
|
| Ammoniums quaternaires |
|
| Composés mercuriels |
|
| Composés de l'ion argent | |
| Alcools | |
| Autres |
|
 Portail de la chimie
Portail de la chimie












