Thiocyanate de guanidinium
| Thiocyanate de guanidinium | |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | thiocyanate de guanidine | ||
| Synonymes | rhodanide de guanidinium | ||
| No CAS | 593-84-0 | ||
| No ECHA | 100.008.922 | ||
| No CE | 209-812-1 | ||
| PubChem | 65046 | ||
| SMILES | C(#N)S.C(=N)(N)N PubChem, vue 3D | ||
| InChI | InChI : vue 3D InChI=1S/CH5N3.CHNS/c2-1(3)4;2-1-3/h(H5,2,3,4);3H InChIKey : ZJYYHGLJYGJLLN-UHFFFAOYSA-N | ||
| Apparence | solide blanc sans odeur[1] | ||
| Propriétés chimiques | |||
| Formule | C2H6N4S [Isomères] | ||
| Masse molaire[2] | 118,161 ± 0,008 g/mol C 20,33 %, H 5,12 %, N 47,42 %, S 27,14 %, | ||
| pKa | pH = 4,8 - 6,0 pour cc 1 420 g/l à 20 °C (solution saturée)[1] | ||
| Propriétés physiques | |||
| T° fusion | 118 °C[1] 120-122 °C[3] | ||
| T° ébullition | décomp. à T > 115 °C[1] | ||
| Solubilité | H2O : 1 420 g/l à 20 °C[1] | ||
| Masse volumique | 1,29 g/cm3 à 20 °C[1] | ||
| Conductivité thermique | W | ||
| Vitesse du son | m/s | ||
| Thermochimie | |||
| S0gaz, 1 bar | J | ||
| S0liquide, 1 bar | J | ||
| S0solide | J | ||
| ΔfH0gaz | kJ/mol | ||
| ΔfH0liquide | kJ/mol | ||
| ΔfH0solide | kJ/mol | ||
| Cp | J | ||
| Précautions | |||
| SGH[3] | |||
  H314 : Provoque de graves brûlures de la peau et des lésions oculaires H412 : Nocif pour les organismes aquatiques, entraîne des effets à long terme H302+H312+H332 : Nocif en cas d'ingestion, par contact cutané ou si inhalé P273 : Éviter le rejet dans l’environnement. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P310 : Appeler immédiatement un CENTRE ANTIPOISON ou un médecin. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. | |||
| Transport[3] | |||
Numéro ONU : 1759 : SOLIDE CORROSIF, N.S.A. Classe : 8 Étiquette :  8 : Matières corrosives Emballage : Groupe d'emballage III : matières faiblement dangereuses. | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
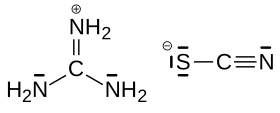
Le thiocyanate de guanidinium ou GITC est un sel composé des cations guanidinium, [CH6N3]+ qui est l'acide conjugué de la guanidine et d'anions thiocyanate. Il est principalement utilisé en biochimie comme agent de dénaturation des protéines général, donc comme agent chaotropique bien qu'il soit le plus communément utilisé pour l'extraction d'ADN et d'ARN[4].
Le thiocyanate de guanidinium peut être aussi utilisé pour désactiver un virus, comme le virus de la grippe qui a provoqué en 1918 la grippe espagnole, de sorte qu'il peut être étudié en toute sécurité. Cette application est vraisemblablement basée sur son activité de dénaturation.
Le thiocyanate de guanidinium est également utilisé pour lyser des cellules et des particules virales pour extraire ARN et ADN, et où, en plus de son action de lyse, il empêche en les dénaturant l'activité d'enzymes RNases et DNases qui pourraient endommager l'extrait.
Une méthode couramment utilisée est l'extraction "thiocyanate de guanidinium-phénol-chloroforme"[5],[6],[7]. Il n'est pas absolument nécessaire d'utiliser du phénol ou du chloroforme, si l'extraction est pour un northern blot ou un Southern blot, car l'électrophorèse sur gel suivie d'un transfert sur une membrane sépare l'ARN/ADN des protéines. En outre, étant donné que ces méthodes (northern ou Southern Blot) utilisent des sondes oligonucléotidiques marquées.[Quoi ?], des peptides qui parviennent à traverser le processus ne sont généralement pas d'importance, sauf si ce peptide a une activité RNase ou DNase, ou et seulement si une enzyme parvient à se renaturer, ce qui ne devrait pas se produire si les protocoles appropriés sont correctement suivis. Une exception possible peut être due à un travail avec des extrêmophiles hyperthermophiles parce que certaines enzymes de ces organismes peuvent rester stables dans des circonstances inhabituelles[8].
Notes et références
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Guanidinium thiocyanate » (voir la liste des auteurs).
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Guanidiniumthiocyanat » (voir la liste des auteurs).
- ↑ a b c d e et f [PDF] (en) feuille de données chez Merck.
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b c et d Fiche Sigma-Aldrich du composé Guanidine thiocyanate for molecular biology, ≥99%, consultée le 24/01/14.
- ↑ P. E. Mason et al., The hydration structure of guanidinium and thiocyanate ions: Implications for protein stability in aqueous solution, PNAS, 2003, vol. 100, no 8, p. 4557–4561. DOI 10.1073/pnas.0735920100.
- ↑ Chomczynski, P. & Sacchi, N., Single-step method of RNA isolation by acid guanidinium thiocyanate-phenol-chloroform extraction., Anal. Biochem., 1987, vol. 162(1), p. 156-159. PMID 2440339.
- ↑ Chomczynski, P. & Sacchi, N., [PDF] The single-step method of RNA isolation by acid guanidinium thiocyanate-phenol-chloroform extraction: twenty-something years on., Nat. Protoc., 2006, vol. 1(2), p. 581-585. PMID 17406285.
- ↑ Classic Protocols : [PDF] Purification of RNA from cells and tissues by acid phenol–guanidinium thiocyanate–chloroform extraction., Nat. Methods., 2006, vol. 3(2), p. 149.
- ↑ Shimomura O, Masugi T, Johnson FH, Haneda Y., Properties and reaction mechanism of the bioluminescence system of the deep-sea shrimp Oplophorus gracilorostris., Biochemistry, 1978, vol. 17(6), p. 994-8. PMID 629957.
 Portail de la chimie
Portail de la chimie  Portail de la biochimie
Portail de la biochimie











