Karbon tetraklorida | |
 |
| Nama |
| Nama IUPAC Karbon tetraklorida
Tetraklorometana |
| Nama lain tetraklorometana, Halon 104 |
| Pengecam |
No. Pendaftaran CAS | - 56-23-5
 Y Y
|
Imej model 3D Jmol | |
| ChEBI | - CHEBI:27385
 Y Y
|
| ChEMBL | - ChEMBL44814
 Y Y
|
| ChemSpider | - 5730
 Y Y
|
| ECHA InfoCard | 100.000.239 |
| Nombor EC | |
| KEGG | - C07561
 Y Y
|
| | |
| Nombor RTECS | |
| UNII | - CL2T97X0V0
 Y Y
|
| Nombor PBB | 1846 |
| | - DTXSID8020250

|
InChI=1S/CCl4/c2-1(3,4)5  Y YKey: VZGDMQKNWNREIO-UHFFFAOYSA-N  Y YInChI=1/CCl4/c2-1(3,4)5 Key: VZGDMQKNWNREIO-UHFFFAOYAV
|
| |
| Sifat |
Formula kimia | CCl4 |
| Jisim molar | 153.82 |
| Rupa bentuk | cecair tidak berwarna |
| Ketumpatan | 1.5842 g/cm3 (Cecair)
1.831 g.cm-3, -186 °C (pepejal)
1.809 g.cm-3, -80 °C (pepejal) |
| Takat lebur | -22.92 °C (250 K) |
| Takat didih | 76.72 °C (350 K) |
Keterlarutan dalam air | 0.8 g/L, 25 °C |
| log P | 2.64 |
| Tekanan wap | 11.94 kPa, 20 °C |
Pemalar hukum Henry (kH) | 365 kJ.mol-1 (24.8°C) |
| Struktur |
| Struktur kristal | monoklinik |
| Bentuk molekul | tetrahedron |
| Bahaya |
| Frasa R | R23/24/25-Templat:R40-Templat:R48/23-Templat:R59-Templat:R52/53 |
| Frasa S | S1/2-Templat:S23-Templat:S36/37-S45-Templat:S59-S61 |
| NFPA 704 (berlian api) | |
| Takat kilat | tidak boleh dibakar |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). |
| Rujukan kotak info |
| | |
Karbon tetraklorida (formula kimia CCl4), juga tetraklorometana ialah sejenis cecair yang tidak berwarna. Dalam sejarah,ia pernah digunakan sebagai pemadam api dan penyejuk. Ia boleh larut dalam alkohol, eter, petroleum eter, nafta, asid asetik, karbon disulfida dan halokarbon. Dalam kalangan semua klorokarbon, sebatian ini ialah racun yang paling kuat.
Penghasilan
Metana dan klorin boleh reaksikan dengan bercahayakannya.Reaksi ini boleh menghasilkan karbon tetraklorida.
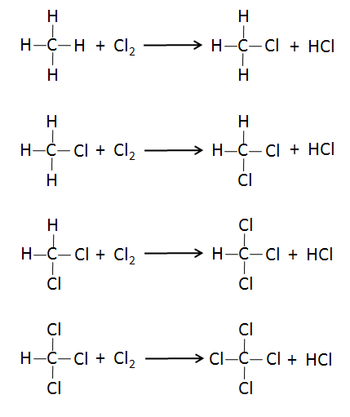
Rujukan
Halometana |
|---|
| Monohalometana | |
|---|
| Dihalometana | - CH2F2
- CH2ClF
- CH2BrF
- CH2FI
- CH2Cl2
- CH2BrCl
- CH2ClI
- CH2Br2
- CH2BrI
- CH2I2
|
|---|
| Trihalometana | - CHF3
- CHClF2
- CHBrF2
- CHF2I
- CHCl2F
- C*HBrClF
- C*HClFI
- CHBr2F
- C*HBrFI
- CHFI2
- CHCl3
- CHBrCl2
- CHCl2I
- CHBr2Cl
- C*HBrClI
- CHClI2
- CHBr3
- CHBr2I
- CHBrI2
- CHI3
|
|---|
| Tetrahalometana | - CF4
- CClF3
- CBrF3
- CF3I
- CCl2F2
- CBrClF2
- CClF2I
- CBr2F2
- CBrF2I
- CF2I2
- CCl3F
- CBrCl2F
- CCl2FI
- CBr2ClF
- C*BrClFI
- CClFI2
- CBr3F
- CBr2FI
- CBrFI2
- CFI3
- CCl4
- CBrCl3
- CCl3I
- CBr2Cl2
- CBrCl2I
- CCl2I2
- CBr3Cl
- CBr2ClI
- CBrClI2
- CClI3
- CBr4
- CBr3I
- CBr2I2
- CBrI3
- CI4
- CAt4
|
|---|
* Sebatian kiral. |
Sebatian karbon bukan organik dan ion berkaitan |
|---|
| Sebatian | - CF
- CO
- CO2
- CO3
- CO4
- CO5
- CO6
- COS
- CS
- C2S2
- CS2
- CSe2
- C3O2
- C3S2
- SiC
|
|---|
| Ion karbon | - Karbida [:C≡C:]2−, [::C::]4−, [:C=C=C:]4−
- Sianida [:C≡N:]−
- Sianat [:O−C≡N:]−
- Tiosianat [:S−C≡N:]−
- Fulminat [:C≡N−O:]−
- Tiofulminat [:C≡N−S:]−
|
|---|
| Nanostruktur | - Sebatian interkalasi grafit
- Fulerida
|
|---|
| Oksida dan ion berkaitan | |
|---|
Garam dan terbitan kovalen ion klorida |
|---|
| HCl | | | | He | | LiCl | BeCl2 | B4Cl4
B12Cl12
BCl3
B2Cl4
+BO3 | C2Cl2
C2Cl4
C2Cl6
CCl4
+C
+CO3 | NCl3
ClN3
+N
+NO3 | ClxOy
Cl2O
Cl2O2
ClO
ClO2
Cl2O4
Cl2O6
Cl2O7
ClO4
+O | ClF
ClF3
ClF5 | Ne | | NaCl | MgCl2 | AlCl
AlCl3 | Si5Cl12
Si2Cl6
SiCl4 | P2Cl4
PCl3
PCl5
+P | S2Cl2
SCl2
SCl4
+SO4 | Cl2 | Ar | | KCl | CaCl
CaCl2 | | ScCl3 | TiCl2
TiCl3
TiCl4 | VCl2
VCl3
VCl4
VCl5 | CrCl2
CrCl3
CrCl4 | MnCl2
MnCl3 | FeCl2
FeCl3 | CoCl2
CoCl3 | NiCl2 | CuCl
CuCl2 | ZnCl2 | GaCl
GaCl3 | GeCl2
GeCl4 | AsCl3
AsCl5
+As | Se2Cl2
SeCl2
SeCl4 | BrCl | Kr | | RbCl | SrCl2 | | YCl3 | ZrCl3
ZrCl4 | NbCl3
NbCl4
NbCl5 | MoCl2
MoCl3
MoCl4
MoCl5
MoCl6 | TcCl3
TcCl4 | RuCl2
RuCl3
RuCl4 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl
InCl2
InCl3 | SnCl2
SnCl4 | SbCl3
SbCl5 | Te3Cl2
TeCl2
TeCl4 | ICl
ICl3 | XeCl
XeCl2
XeCl4 | | CsCl | BaCl2 | * | LuCl3 | HfCl4 | TaCl3
TaCl4
TaCl5 | WCl2
WCl3
WCl4
WCl5
WCl6 | ReCl3
ReCl4
ReCl5
ReCl6 | OsCl2
OsCl3
OsCl4
OsCl5 | IrCl2
IrCl3
IrCl4 | PtCl2
PtCl4 | AuCl
(Au[AuCl4])2
AuCl3 | Hg2Cl2
HgCl2 | TlCl
TlCl3 | PbCl2
PbCl4 | BiCl3 | PoCl2
PoCl4 | AtCl | Rn | | FrCl | RaCl2 | ** | LrCl3 | RfCl4 | DbCl5 | SgO2Cl2 | BhO3Cl | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | | | | | * | LaCl3 | CeCl3 | PrCl3 | NdCl2
NdCl3 | PmCl3 | SmCl2
SmCl3 | EuCl2
EuCl3 | GdCl3 | TbCl3 | DyCl2
DyCl3 | HoCl3 | ErCl3 | TmCl2
TmCl3 | YbCl2
YbCl3 | | ** | AcCl3 | ThCl4 | PaCl4
PaCl5 | UCl3
UCl4
UCl5
UCl6 | NpCl3 | PuCl3 | AmCl2
AmCl3 | CmCl3 | BkCl3 | CfCl3 | EsCl2
EsCl3 | FmCl2 | MdCl2 | NoCl2 | |
Kawalan kewibawaan: Perpustakaan negara  | - Jerman
- Israel
- Amerika Syarikat
- Latvia
- Jepun
- Republik Czech
|
|---|












